
微信扫一扫
关注公众号
AAV基因传递系统介绍
发布时间:2019-11-03 22:10 | 点击次数:1726
什么是AAV?
腺相关病毒AAV(Adeno-associated virus)属于细小病毒科,是最小的单链和非包膜DNA病毒之一,仅由核酸和蛋白衣壳组成。正因为病毒的结构简单,所以它需要寄生在活细胞内才能进行繁殖。由于需要进入活细胞内繁殖,所以病毒都练就了一身破膜进入胞内的本领。基于这种能力,科学家开发了病毒基因传递系统。该系统利用病毒作为载体,可以把外源治疗基于带到细胞内部完成基因治疗的关键步骤。目前比较成熟的病毒基因传递系统主要包括逆转录病毒(RV)、腺病毒(AdV)、腺相关病毒(AAV)、慢病毒(LV)和单纯疱疹病毒(HSV)。
AAV的基因组
通过基因组研究发现AAV有一个大约4.7 kb的线性单链DNA (ssDNA)基因组,在末端有两个145个核苷酸长反向末端重复(ITR)。该病毒不编码聚合酶,因此依赖于细胞聚合酶进行基因组复制。ITRs位于两个病毒基因rep(复制)和cap(衣壳)的侧面,分别编码非结构蛋白和结构蛋白。cap基因通过选择性剪接和翻译起始,分别产生三种衣壳蛋白VP1(病毒蛋白1)、VP2和VP3。这些衣壳蛋白组装成60个亚基的近球形蛋白外壳。rep基因通过两个启动子和选择性剪接,编码四种调节蛋白,分别称为Rep78、Rep68、Rep52和Rep40。这些蛋白参与了AAV基因组的复制。
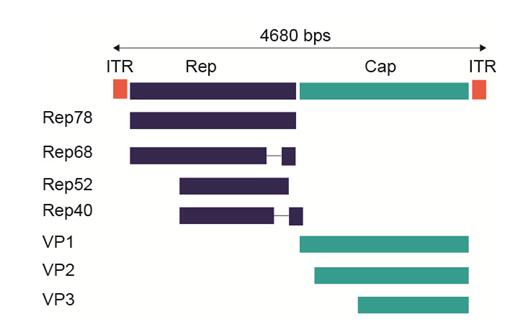
图1. AAV2的基因图谱
AAV的特性
作为本次介绍的主角,AAV具有与其他病毒基因传递系统不同的三大主角光环:1 AAV在感染人类和其他灵长类动物时只能在体内引起非常轻微的免疫反应;2使用AAV作为基因治疗载体时不仅可以感染正常分裂的细胞,而且还可以感染休眠的细胞;3进入细胞的AAV装载的核酸可以不整合到基因组上,进而保持染色体外状态,这样可以防止由于外来基因片段插入造成基因组不稳定。这些特性使AAV成为基因治疗、病毒载体和人类同基因疾病模型的诱人的候选对象。
AAV的特性是如何产生的呢?
野生型AAV由于其诸多特性,引起了基因治疗研究者的极大兴趣。那这些特性是如何产生的呢?其中关于AAV装载的核酸可以不整合到基因组上这一特性已经研究的比较清楚。研究发现一般天然AAV可以稳定地整合到人类19号染色体的一个特定位置(AAVS1)。这一特性使它比具有随机插入和诱变威胁的逆转录病毒更可预测。而有趣的是,AAV还可以通过从载体的DNA中去除rep和cap序列来消除这种整合能力进而使装载的DNA不会整合到基因组中。通过宿主细胞DNA聚合酶复合物将单链载体DNA转化为双链后,在倒末端重复序列(ITR)之间插入一个驱动基因转录的所需基因和一个启动子,倒末端重复序列有助于在细胞核内形成连接体。在未分裂的细胞中,这些结合物在宿主细胞的生命周期中保持完整。
如何选择AAV血清型?
研究发现,AAV有多种血清型。不同血清型的AAV载体之间的主要区别是衣壳蛋白不同。目前,基因传递中最常见的AAV血清型为AAV1、AAV2、AAV5、AAV6、AAV8、AAV9。不同的血清型对不同细胞和组织的转染效率不同。因此,选择合适的AAV血清型至关重要。
通过临床实验结果表明: AAV1对肌肉、肝脏和血管内皮的感染更优;AAV2对骨骼肌、神经元、血管平滑肌细胞、肺泡细胞和肝细胞具有天然的趋向性;AAV5在小鼠气道和肺泡上皮细胞的转化效率较AAV2高;AAV6载体在大气道和小气道的上皮细胞转导效率AAV2高;AAV8型显示出更大的肝脏转导效率;AAV9具有跨过血脑屏障的能力。所以在选择AAV血型的时候,需要考虑我们转化的组织和细胞的特性,然后确定合适的AAV类型。
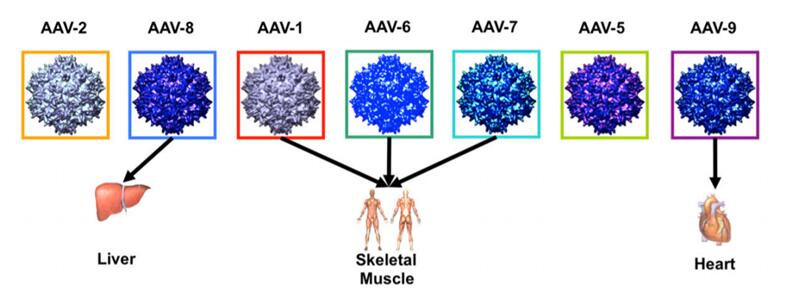
图2. 基因转移最常用的AAV载体以及其天然趋向性。
如何检测AAV制剂的质量
当完成AAV制剂之后,我们不能直接拿来使用。因为只有通过质量检测合格的制剂,我们才能保证后续实验的成功。目前,对AAV制剂进行鉴定的方法主要包括:滴定ELISA、qPCR、ddPCR、DNA斑点杂交、转换单元的测定、感染中心测定、SDS-PAGE或电镜等。qPCR已被广泛使用,但仍存在一些问题,例如样品制备,引物设计或PCR效率,这些问题可能导致实验室间结果之间的高度差异。数字液滴PCR方法克服了qPCR的某些局限性。但是,由于不同的样品处理方案,实验室之间仍然可能发生变化。如果使用可靠的参照,则斑点印迹是一种简单且定量的方法。然而,它通常受蛋白质印迹的线性和动态范围的限制。考虑到上述技术的实际缺陷,目前常规的夹心ELISA在实验室间和实验室间的变异以及易于使用方面似乎是优越的。因此,它代表了可靠和可再现的总rAVV衣壳滴度定量的最佳方法。
产品推荐
我们提供基于夹心法ELISA的AAV滴度检测试剂盒和不同亚型的AAV抗体,可特异性识别完整的病毒衣壳;腺相关病毒亚基或AAV复制酶。
参考文献:
-
Colella P. et al. Emerging Issues in AAV-Mediated In Vivo Gene Therapy. Mol Ther Methods Clin Dev. 2017, 8:87-104.
-
Berns KI. et al. AAV: An Overview of Unanswered Questions. Hum Gene Ther. 2017, 28(4):308-313.
-
Barnes C. et al. Engineering the AAV capsid to evade immune responses.Curr Opin Biotechnol. 2019, 60:99-103.









