
微信扫一扫
关注公众号
荧光原位杂交实验Protocol
发布时间:2019-10-20 17:46 | 点击次数:2021
荧光原位杂交(fluorescence in situ hybridization)简称FISH,是指用已知的荧光素标记的单链核酸为探针,按照碱基互补配对的原则,与待检测材料中未知的单链核酸进行特异性结合,形成可被检测的杂交双链核酸。随后在荧光显微镜下进行定性、定量或相对定位分析。与传统的放射性标记原位杂交相比,荧光原位杂交具有快速、检测信号强、杂交特性高和可以多重染色等特点,因此在分子细胞遗传学领域受到普遍关注。很多公司有探针和成服务,可以直接找公司购买荧光标记的探针,也可以自己通过PCR等方法自行制备。
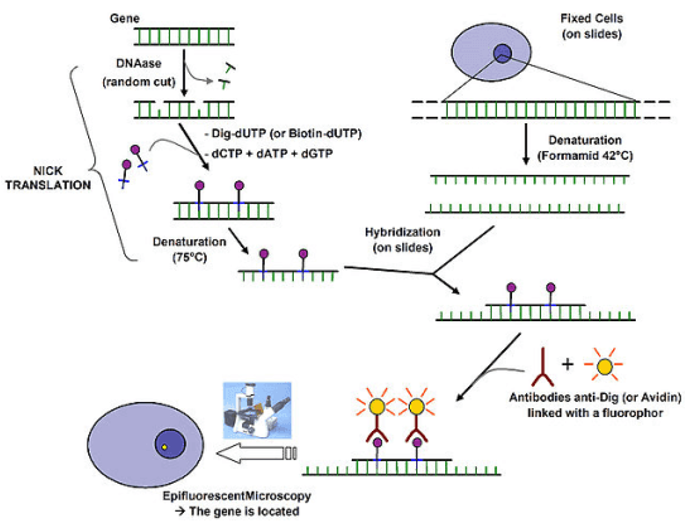
图1. 荧光原位杂交示意图.
下面是我们以Y染色体探针与人外周血细胞中期染色体标本为例,进行荧光原位杂交的实验操作详解。
实验材料:
Y染色体探针(通过缺口平移法制备的biotin标记探针)
人外周血细胞中期染色体标本
实验试剂:
NaCl、NaOH、柠檬酸钠、甲酰胺、吐温20、指甲油,avidin-FITC,anti-avidin,乙醇
仪器、耗材:
培养箱、恒温水浴锅、载玻片、盖玻片、染色缸、封口膜、移液器、暗盒、荧光显微镜
相关溶液配制:
1、20×SSC:175.3g NaCl, 88.2g柠檬酸钠,加水至1000mL(用10mol/L NaOH调pH至7.0)。
2、去离子甲酰胺(DF):将10g混合床离子交换树脂加入100mL甲酰胺中。电磁搅拌30min,Whatmanl号滤纸过滤,棕色瓶保存。
3、70%(v/v)甲酰胺/2×SSC:35mL甲酰胺,5mL 20×SSC,10mL水。
4、50%(v/v)甲酰胺/2×SSC:100mL甲酰胺,20mL 20×SSC,80mL水。
5、50%(v/v)硫酸葡聚糖(DS):65℃水浴中融化,4℃或-20℃保存。
6、杂交液(体积分数10% DS,50% DF,2×SSC):8mL体积分数25%DS, 20mL 20×SSC,混合,然后取上述混合液50mL,与5mL DF混合即成,需现配现用。
7、PI/antifade溶液
-
PI原液:先以双蒸水配置溶液,浓度为100mg/mL,取出1mL,加39mL双蒸水,使其终浓度为2.5mg /mL。
-
Antifade原液:以PBS缓冲液配制该溶液,使其浓度为10mg/mL,用0.5mmol/L的NaHCO3调pH值为8.0。取上述溶液1mL,加9mL甘油,混匀。
-
PI/antifade溶液:PI与antifade原液按体积比1:9比例充分混匀,-20℃保存备用。
8、封闭液I:体积分数5% BSA 3mL,20×SSC 1mL,dd H2O 1mL, Tween 20 5mL,混合。
9、封闭液II:体积分数5% BSA 3mL,20×SSC 1mL,goat serum 250mL, dd H2O 750mL, Tween 20 5mL,混合。
10、洗脱液:100mL 20×SSC,加水至500mL,再加Tween20 500 mL。
实验步骤:
1、探针变性
将探针在75℃恒温水浴中温育5min,立即置0℃,5~10min,使双链DNA探针变性。
2、标本变性
(1)将制备好的染色体玻片置于50℃培养箱中,烤片2~3h。
(2)取出玻片标本,浸于70~75℃、体积分数70%甲酰胺/2×SSC的变性液中变性2~3min。
(3)按顺序将标本经体积分数70%、90%和100%的冰乙醇系列脱水,每次5min,然后空气干燥。
3、杂交
将已变性的DNA探针10µL滴于已变性脱水的玻片标本上,盖上盖玻片,用Parafilm(封口膜)小心封片,置于潮湿暗盒中,37℃培养箱中杂交过夜(约15~17h)。由于杂交液较少,而且杂交温度较高,持续时间又长,因此为了保持标本的湿润状态,此过程在湿盒中进行。
4、洗脱
(1)杂交次日,将标本从37℃培养箱中取出,轻轻揭掉盖玻片。
(2)将已杂交的玻片标本置于42~50℃的体积分数50%甲酰胺/2×SSC中洗涤3次,每次5min。
(3)在42~50℃的1×SSC中洗涤3次,每次5min。
(4)室温下,将玻片标本置于2×SSC中轻洗一下。
此步骤有助于除去非特异性结合的探针,从而降低背景。
5、杂交信号的放大
(1)加150µL封闭液I,用保鲜膜覆盖,37℃温育20min。
(2)去掉保鲜膜,再加150µL avidin-FITC于标本上,用保鲜膜覆盖,37℃继续温育40min。请注意,后续的步骤都需要避光处理!!
(3)取出标本,将其放入42~50℃的洗脱液中洗涤3次,每次5min。
(4)加150µL封闭液II,覆盖保鲜膜,37℃温育20min。
(5)去掉保鲜膜,加150µL anti-avidin于标本上,覆盖新的保鲜膜,37℃温育40min。
(6)取出标本,将其放入42~50℃的新洗脱液中,洗涤3次,每次5min。
(7)重复步骤(1)、(2)、(3),再于室温下2×SSC中清洗一下。
(8)取出玻片,自然干燥。
(9)将200µL PI/antifade染液滴加在玻片标本上,盖上盖玻片。
6、封片
可采用不同类型的封片液。如果封片中不含有Mowiol(可使封片液产生自封闭作用),为防止盖玻片与载玻片之间的溶液挥发,可使用指甲油将盖玻片周围封闭。封好的玻片标本可以在-20~-70℃的冰箱中的暗盒中保持数月之久。
7、荧光显微镜镜检
先在可见光源下找到具有细胞分裂相的视野,然后打开荧光激发光源,经FITC标记的探针所在位置发出绿色荧光。
附:探针的生物素标记
本实验采用缺口平移法,以biotin-14-dATP标记探针。标记好的探针可以在-20℃下长期保存。
1、10X dNTP:500 mmol/L Tris · HCl (pH 7.8), 50 mmol/L MgCl2, 100 mmol/L β-硫基乙醇, 100 mg/ml去除核酸酶的牛血清白蛋白, 0.2 mmol/L dCTP, 0.2 mmol/L dGTP, 0.2 mmol/L dTTP, 0.1 mmol/L dATP, 0.1 mmol/L biotin-14-dATP。
2、10X Enzyme Mix: 0.5 units/mL DNA聚合酶I, 0.075 units/mL Dnase I, 50 mmol/L Tris · HCl(pH 7.5), 5 mmol/L醋酸镁, 1 mmol/L β-硫基乙醇, 0.1 mmol/L PMSF, 50%(v/v)甘油, 100 mg/mL牛血清白蛋白。
3、总反映体积50 mL:DNA 1 mg, 10X dNTP 5 mL, 10X Enzyme Mix 5 mL。
4、将上述混合液于16℃作用1 h。用8.0 g/L琼脂糖/TBE缓冲液凝胶电检测标记产物。以DNA片段长约300~500 bp为宜。如片段较大,则应加适量Dnase I继续酶切,直至DNA片段长度适中后,加5mL终止缓冲液(300mmol/L EDTA)终止反应。用乙醇沉淀的方法将探针与非掺入的核苷酸分开。









